Sections
- Gestion des effluents dans la production de médicaments
- Production d’eaux usées dans l’industrie pharmaceutique
- Traitement des déversements avec des contaminants émergents
- Processus d’oxydation avancée (POA) + Traitements biologiques
- Évaporation sous vide
- Oxydation avancée (POA) + Évaporation
- Évaporateurs sous vide pour la récupération de principes actifs (API) dans les effluents résiduels
- Résumé
Gestion des effluents dans la production de médicaments
Chaque année, plus de 100 000 tonnes de produits pharmaceutiques sont consommées dans le monde. Les principes actifs pharmaceutiques (API) sont à l’origine de la pollution environnementale, tant lors de leur fabrication que plus tard pendant leur utilisation et leur élimination.
Les eaux usées générées dans ce secteur sont très variables en termes de débit et de composition, ce qui rend le traitement complexe.
Il existe diverses technologies pour le traitement biologique de ces déversements, parmi lesquelles se distinguent : le traitement biologique par boues activées, le processus biologique MBBR (biomasse fixe sur lit mobile), les traitements anaérobies, les traitements sélectifs de micro-contaminants, etc.
Le problème est que dans de nombreux cas, des problèmes provoqués par des contaminants inhibiteurs et toxiques apparaissent, ainsi que par des composés organiques résistants à l’oxydation.
Pour cette raison, de nombreuses entreprises de l’industrie pharmaceutique confient la gestion de leurs effluents à des gestionnaires de déchets spécialisés, entraînant des coûts élevés pour l’élimination de leurs déchets liquides.
Dans ce contexte, les évaporateurs sous vide se distinguent par leur rendement élevé et leur rentabilité économique lors du traitement des eaux usées produites par l’industrie pharmaceutique.
Production d’eaux usées dans l’industrie pharmaceutique
Dans le secteur pharmaceutique, de l’eau purifiée est utilisée pour la fabrication de ses produits spécifiques et, d’autre part, de l’eau d’appoint est également utilisée pour les processus de nettoyage des équipements, des récipients et des emballages primaires. En conséquence, des effluents sont obtenus, caractérisés par la présence de résidus de produits chimiques, tels que des restes de médicaments et/ou des détergents utilisés lors du nettoyage.
L’Organisation mondiale de la santé indique qu’une grande diversité de déchets générés par le secteur pharmaceutique se mélange à l’eau de l’environnement, à travers les effluents des installations de fabrication ou de production.
Le volume et la composition des eaux usées provenant de cette industrie présentent une grande variabilité en raison des différentes modalités dans les processus de production et de la composition des médicaments.
Dans les processus de fabrication de produits pharmaceutiques, des substances contenant des produits chimiques, des produits de nettoyage et les dits API, ou principes actifs, qui sont la base des médicaments commercialisés pour la prévention et le traitement des maladies, sont utilisés.
Ces contaminants anormaux pour l’environnement sont appelés « contaminants émergents » (CE), et ce sont des composés qui sont déversés dans l’eau et qui ne sont pas réglementés. Les contaminants émergents, également appelés micro-contaminants, sont des composés chimiques issus des activités humaines réalisées dans la vie quotidienne, comme l’hygiène personnelle ou le soin de la santé. Ce sont des substances d’origines et de compositions chimiques différentes dont on sait relativement peu sur l’impact qu’elles ont sur l’environnement et sur l’être humain.
Traitement des déversements avec des contaminants émergents
En général, les processus de traitement biologique sont les plus économiques et courants pour le traitement des eaux usées, mais la complexité des composants présents dans les eaux usées de l’industrie pharmaceutique rend l’application d’un traitement particulier difficile. De même, la présence de certains composés comme les antibiotiques et les désinfectants empêche une élimination complète des contaminants par les traitements biologiques conventionnels.
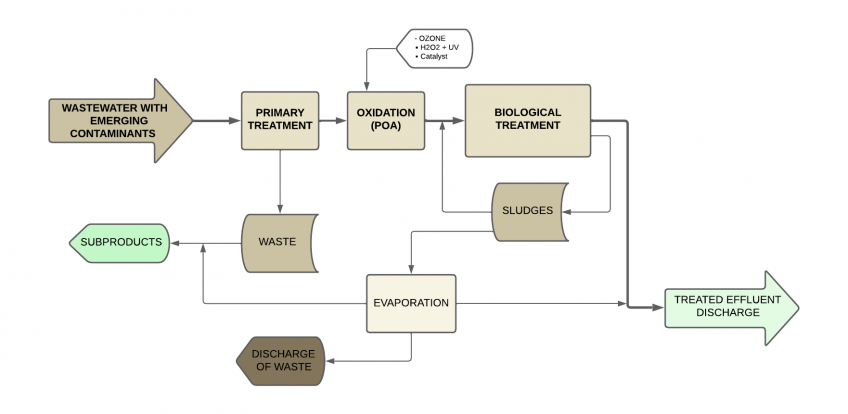
Processus d’oxydation avancée (POA) + Traitements biologiques
Les processus d’oxydation avancée (POA) ont montré une grande efficacité pour les eaux usées produites dans l’industrie pharmaceutique, en particulier celles contenant des micro-contaminants ou des contaminants émergents.
Cette technologie utilise des oxydants chimiques pour réduire les niveaux de demande chimique en oxygène (DQO), ainsi que pour rompre les liaisons de ces composés organiques contaminants et faciliter leur biodégradabilité, ce qui permet d’économiser des réactifs et de réduire les coûts d’exploitation par rapport à une oxydation de toute la matière organique avec des réactifs.
Ces traitements reposent sur des processus physico-chimiques capables de produire des changements profonds dans la structure chimique des contaminants, impliquant la génération et l’utilisation d’espèces transitoires puissantes, principalement le radical hydroxyle (OH-), qui a le plus grand pouvoir oxydant après le fluor. De plus, la génération de radicaux se fait à partir d’oxygène, d’eau oxygénée et de catalyseurs supportés, de sorte que les sous-produits de réaction sont uniquement de l’eau et du dioxyde de carbone.
Parmi les principales technologies de processus d’oxydation avancée, on trouve les processus de Fenton et ses variantes, qui consistent en l’ajout de sels de fer agissant comme catalyseurs, en présence de peroxyde d’hydrogène (HO), en milieu acide, et dans des conditions spécifiques de pression et de température, pour la formation de radicaux OH-.
Après le processus POA, un traitement biologique peut être poursuivi, ce qui dans de nombreux cas permettra de respecter les limites de déversement, et même de réutiliser les eaux traitées dans les services de l’industrie elle-même, ou pour l’irrigation.
Évaporation sous vide
L’évaporation sous vide est un processus qui implique l’élimination de l’eau et d’autres solvants présents dans un résidu liquide par l’application de chaleur sous des conditions de vide.
En réduisant la pression atmosphérique sur la solution, le point d’ébullition du liquide est abaissé, ce qui permet son évaporation à des températures plus basses.
Contributions du processus
L’évaporation sous vide est une technologie largement utilisée par l’industrie pharmaceutique. Voici un résumé de la manière dont ce processus contribue à la gestion des eaux usées générées dans cette industrie :
- Concentration des contaminants et minimisation de l’effluent résiduel : Pendant l’évaporation, l’eau est chauffée et se transforme en vapeur. Les contaminants organiques et inorganiques présents dans l’eau ne s’évaporent pas et restent concentrés dans la solution résiduelle. Cela permet de réduire le volume total des eaux usées qui doivent être traitées ultérieurement et de séparer une partie importante des contaminants.
- Récupération de produits précieux et réutilisation de l’eau : Les produits concentrés peuvent être précieux pour les industries qui les génèrent, comme c’est le cas des API pour les industries pharmaceutiques. Leur récupération nécessite un processus d’évaporation contrôlé dans des conditions d’exploitation spécifiques pour éviter qu’ils ne se détériorent ou perdent leurs qualités.
- Élimination des micro-contaminants : Bien que l’évaporation n’élimine pas complètement les micro-contaminants, elle peut les concentrer. Par la suite, des techniques supplémentaires (comme l’adsorption ou la filtration) peuvent être appliquées pour éliminer ces contaminants concentrés.
- Efficacité énergétique : Les évaporateurs sous vide ont amélioré leur efficacité opérationnelle afin de réduire la consommation énergétique, comme c’est le cas des évaporateurs avec pompes à chaleur, ou ceux qui fonctionnent avec compression thermique de vapeur.
Limitations du processus
L’évaporation est une technique précieuse dans le traitement des eaux usées de l’industrie pharmaceutique, mais elle a aussi ses limitations. Voici quelques-unes d’entre elles :
- Complexité des effluents : Les eaux usées pharmaceutiques peuvent contenir une variété de composés, y compris des principes actifs pharmaceutiques (API), des produits chimiques et des micro-contaminants. L’évaporation ne peut pas toujours éliminer tous ces composants de manière efficace en raison de leur complexité.
- Concentration des contaminants : Bien que l’évaporation concentre les contaminants dans le rejet (la fraction non évaporée) et minimise le volume de déchets à envoyer à un gestionnaire, ce rejet de composés concentrés peut rester nuisible pour l’environnement et doit être géré correctement.
- Limitations dans l’élimination des micro-contaminants : Bien que l’évaporation puisse concentrer les micro-contaminants, elle ne les élimine pas toujours complètement. Des étapes supplémentaires peuvent être nécessaires pour traiter ces composés spécifiques.
- Besoin de technologies complémentaires : Pour surmonter les limitations de l’évaporation, elle est souvent combinée avec d’autres techniques de traitement, telles que l’adsorption ou la biodégradation. Le choix de la technologie appropriée dépend de la composition spécifique des eaux usées.
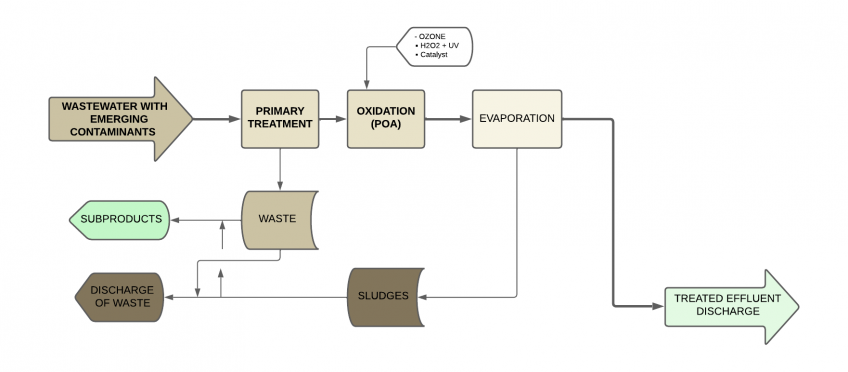
Oxydation avancée (POA) + Évaporation
La combinaison d’oxydation avancée et d’évaporation sous vide est une solution de haute performance pour le traitement des eaux usées générées par l’industrie pharmaceutique.
Les Processus d’Oxydation Avancée (POA) sont des méthodes qui utilisent des radicaux hydroxyles (OH-) hautement réactifs pour oxyder et dégrader les contaminants organiques. Ces processus présentent des avantages tels que la capacité de minéraliser des composés organiques et la réactivité avec une large gamme de contaminants.
Cependant, les processus d’oxydation avancée ont également des inconvénients, tels que le coût des réactifs et les exigences énergétiques. Par conséquent, ils sont souvent combinés avec d’autres traitements.
L’évaporation sous vide, comme nous l’avons mentionné, est une technique qui concentre les contaminants en transformant l’eau en vapeur. Elle peut réduire le volume total des eaux usées et permettre la récupération de produits précieux. Cependant, l’évaporation a également des coûts énergétiques et n’élimine pas complètement les micro-contaminants.
La combinaison de POA et d’évaporation offre une haute efficacité, car les POA peuvent dégrader des composés organiques difficiles à traiter, et l’évaporation peut concentrer les contaminants avant d’appliquer d’autres traitements. Cette combinaison de processus est particulièrement adaptée aux faibles débits et aux fortes charges contaminantes.
Évaporateurs sous vide pour la récupération de principes actifs dans les effluents résiduels
Les API sont des substances chimiques qui doivent être manipulées avec une extrême précaution en raison de leur impact potentiel sur la santé publique. Un traitement inadéquat des API peut entraîner des problèmes tels que :
- La contamination croisée
- La perte de puissance du médicament, ou
- La présence d’impuretés, ce qui pourrait mettre en danger la santé des patients et compromettre la réputation de l’entreprise pharmaceutique.
Les processus de production des API suivent le schéma de base suivant :
- Réception et stockage : Les API arrivent généralement dans les installations de l’entreprise pharmaceutique sous forme de poudre, de granulés ou de liquides. Il est crucial de disposer de procédures rigoureuses pour la réception et le stockage de ces matériaux, garantissant leur identification correcte, leur intégrité et leur traçabilité.
- Manipulation et traitement : Lors de la fabrication de médicaments, les API sont manipulés et traités pour formuler les produits finaux. Ce processus comprend des opérations telles que le mélange, la granulation, la compression et l’encapsulation, qui doivent être effectuées selon des protocoles stricts de bonnes pratiques de fabrication (BPF).
- Analyse et contrôle de qualité : Des analyses approfondies sont réalisées pour vérifier l’identité, la pureté et la puissance des API, ainsi que pour détecter la présence d’impuretés. Ces contrôles de qualité sont essentiels pour garantir que les médicaments respectent les normes réglementaires et soient sûrs pour leur utilisation.
- Stockage et distribution : Les API terminés doivent être stockés dans des conditions appropriées pour préserver leur stabilité et éviter la contamination. De plus, des procédures sûres doivent être établies pour la distribution des API vers d’autres installations de fabrication ou vers les clients finaux.
La fabrication d’API est soumise à des contrôles stricts de la part des agences réglementaires. Il est crucial que les entreprises respectent ces réglementations et appliquent de bonnes pratiques de fabrication pour garantir la qualité et la sécurité des produits pharmaceutiques.
Ces composés, ainsi que d’autres ingrédients chimiques, sont libérés dans l’environnement par le biais des eaux usées, créant un problème qui doit être abordé dès l’origine, c’est-à-dire pendant le processus de production, par l’utilisation de technologies efficaces pour gérer ces effluents résiduels.
Dans ce sens, les entreprises prennent de plus en plus conscience de la nécessité de suivre une politique environnementale durable et recherchent des solutions qui permettent de minimiser non seulement le volume des déchets produits, mais aussi d’améliorer l’efficacité de leur élimination.
Les traitements des eaux usées conventionnels n’arrivent pas toujours à éliminer tous les résidus de principes actifs pharmaceutiques, car il s’agit de déchets très complexes à traiter.
Les évaporateurs sous vide sont la technologie la plus efficace pour séparer, concentrer et réutiliser les API, ainsi que d’autres contaminants, présents dans les eaux usées produites par l’industrie pharmaceutique.

Les avancées technologiques réalisées ces dernières années ont permis de réduire les coûts opérationnels des évaporateurs sous vide, les rendant ainsi une technologie capable de répondre à la nécessité de traiter des effluents complexes, comme ceux produits dans le secteur pharmaceutique.
La séparation des principes actifs pharmaceutiques (API) par évaporation est une méthode utilisée dans l’industrie pharmaceutique pour purifier ou concentrer des substances chimiques. Ce processus implique l’évaporation contrôlée du solvant dans lequel le principe actif est dissous, laissant derrière lui le composé que l’on souhaite récupérer sous forme solide ou concentrée.
Les évaporateurs sous vide permettent de concentrer et de récupérer les API utilisés par l’industrie pharmaceutique, comme c’est le cas des solvants ou des produits chimiques utilisés dans la synthèse de médicaments.
Le processus d’évaporation peut être réalisé de plusieurs manières :
- Évaporation sous vide
- Évaporation à température ambiante
- Évaporation par chauffage.
Le choix de la méthode dépend des propriétés du principe actif et du solvant utilisé, ainsi que des exigences spécifiques du processus.
L’évaporation sous vide est une technique efficace pour la séparation et la concentration des principes actifs, mais il est important que le processus se déroule dans des conditions appropriées pour éviter la dégradation ou la perte de pureté du composé d’intérêt.
Par conséquent, il faut prendre en compte des facteurs tels que :
- Température : La température d’évaporation varie selon le principe actif et le solvant utilisé. En général, une température suffisamment élevée est choisie pour favoriser une évaporation efficace du solvant, mais suffisamment basse pour éviter la dégradation ou la volatilisation du principe actif. Par conséquent, les températures se situent généralement dans une plage ambiante à modérément élevées, en fonction des besoins du processus et de la stabilité du composé.
- Pression : La pression peut également varier en fonction des conditions spécifiques du processus. Dans de nombreux cas, une pression réduite ou sous vide est utilisée pour faciliter l’évaporation à des températures plus basses, ce qui aide à prévenir la dégradation thermique du principe actif et du solvant. La pression réduite abaisse le point d’ébullition du solvant, ce qui facilite son évaporation à des températures plus basses.
- Temps d’exposition : Le temps pendant lequel le principe actif est maintenu dans des conditions d’évaporation est également important. Un équilibre est recherché entre l’élimination efficace du solvant et la minimisation de l’exposition du principe actif à des conditions pouvant provoquer sa dégradation.
L’évaporation des principes actifs pharmaceutiques (API) peut être réalisée dans différentes conditions de pression et de température, en fonction des propriétés physiques et chimiques du principe actif et du solvant, ainsi que des exigences spécifiques du processus.
En résumé, l’évaporation des principes actifs pharmaceutiques se fait généralement à des températures modérées, avec des pressions réduites ou sous vide pour faciliter l’évaporation et minimiser la dégradation, et avec des temps d’exposition contrôlés pour garantir la qualité du produit final.
Pour l’évaporation des principes actifs pharmaceutiques (API) sous vide, plusieurs types d’évaporateurs peuvent être utilisés, adaptés aux besoins spécifiques de l’application :
- Évaporateurs à film descendant sous vide : Ces évaporateurs utilisent un design à film descendant pour maximiser l’efficacité du transfert de masse et de chaleur. Ils sont adaptés à la concentration de solutions visqueuses et sensibles à la chaleur, car ils permettent un temps de résidence court et une évaporation douce.
- Évaporateurs à effet multiple : Ils permettent d’atteindre de fortes concentrations dans les produits à déshydrater en agissant avec effet multiple.
- Évaporateurs avec pompe à chaleur : Ils permettent d’évaporer le déchet contenant le produit à déshydrater, à basse température et sous des conditions de pression dans un temps d’exposition modéré. Ils sont adaptés à la concentration de solutions de haute viscosité et d’API susceptibles de se dégrader à des températures élevées.
- Cristalliseurs sous vide avec pompe à chaleur : Avec ces équipements, on obtient des valeurs de concentration élevées du produit à séparer et à sécher, avec une faible consommation et un rendement élevé, tout en respectant la stabilité des composés API.
En général, le choix de l’évaporateur approprié dépendra de plusieurs facteurs, tels que les propriétés du principe actif et du solvant, le volume de l’échantillon, la sensibilité à la chaleur et les exigences spécifiques du processus. Il est important de sélectionner un évaporateur qui offre un contrôle précis de la température et de la pression d’évaporation, ainsi qu’une haute efficacité de transfert de masse, pour garantir une évaporation efficace et une haute qualité du produit final.
Conclusion
La fabrication de médicaments et le nettoyage des équipements génèrent des eaux usées avec des contaminants émergents (CE) difficiles à éliminer par des traitements traditionnels.
Parmi les diverses technologies disponibles, l’évaporation sous vide se présente comme une solution efficace et rentable pour traiter les déversements de l’industrie pharmaceutique, bien qu’il soit important de considérer ses limitations et de la combiner avec d’autres stratégies pour parvenir à une gestion intégrale et responsable de ces eaux usées complexes.
Dans un contexte de prise de conscience environnementale croissante et de réglementations plus strictes, il est prévu que l’évaporation sous vide reste une option attrayante pour le traitement des déversements dans l’industrie pharmaceutique.
Bibliographie et consultations :
Traitement des eaux usées de l’industrie pharmaceutique par la technique de l’ozone
Traitement des eaux usées industrielles | Condorchem Enviro Solutions
