Chapitres
- Définition
- Caractéristiques du procédé
- Sélectivité de la membrane
- Problèmes spécifiques d’encrassement
- Applications générales
- Applications industriels
Definitión
L’osmose (O) et l’osmose inversée (RO) sont deux phénomènes qui se produisent naturellement à l’intérieur des êtres vivants.
Par exemple, grâce à l’osmose les cellules de notre organisme qui sont enveloppées par une membrane semi-perméable permettent le passage des nutriments dans et hors de la cellule, ce qui favorise autant l’incorporation de nutriments nécessaires au métabolisme cellulaire, ainsi que l’expulsion de leurs déchets.
Dans cet article nous nous centrons sur le processus d’Osmose Inversée (RO), qui consiste généralement à produire, grâce à une membrane perméable à l’eau, une solution aqueuse à faible teneur en sel à partir d’une autre à haute teneur en sel et qui en aucun cas n’est un processus de filtrage au travers de la membrane, comme ce serait le cas pour le microfiltrage ou l’ultrafiltrage, mais le solvant se diffuse au travers de la membrane.
Caractéristiques du procédé
La technique de RO a grandement évolué sur les dernières décennies et elle passé du statut de technologie émergente à un processus consolidé, efficace et compétitif. Cependant, en quoi consiste exactement l’osmose inversée ? Pour répondre à cette question, nous analyserons avant tout en quoi consiste le processus d’osmose.
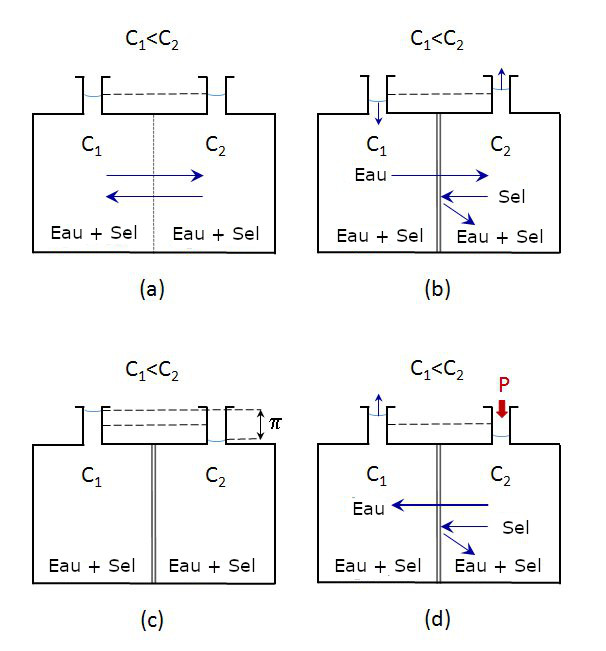
En prenant en compte ces préalables, on peut dire que l’osmose (O) est une opération d’équilibre dans laquelle des molécules d’un solvant sont capables de traverser une membrane perméable pour diluer une solution plus concentrée. Si l’on dispose d’un appareil comme celui de l’illustration (a) dans lequel se trouvent deux solutions à différente concentration de sel à pression atmosphérique qui sont séparées par une barrière physique, au moment où la barrière qui les sépare est retirée, une diffusion naturelle se produit et les concentrations des deux solutions s’égalisent, c’est à ce moment que l’on parvient à l’équilibre. Au début, il y aura un flux qui sera majoritaire et qui ira de la solution la plus dissoute à la plus concentrée, mais à mesure que les concentrations s’égalisent, les flux se rejoignent et le flux net sera zéro.
Sur l’illustration (b) on dispose du même montage expérimental, mais maintenant les eux solutions sont séparées par une membrane semi-perméable, laquelle laisse passer le solvant, mais pas les ions ni les molécules de grande taille. Dans ce cas, le phénomène de l’osmose se produit à nouveau, le solvant de la solution plus diluée traverse la membrane vers la solution plus concentrée.
En revanche, les ions de la solution plus concentrée ne pouvant pas traverser la membrane restent confinés. Suite à ce transfert de solvant d’un côté à l’autre de la membrane, dans la partie supérieure des réservoirs, on observe comment le niveau des deux solutions a changé. Tandis que le niveau de la solution plus diluée a diminué, le niveau de la solution plus concentrée a augmenté.
Une fois que le flux s’est arrêté -illustration (c)- et le niveau des deux réservoirs ne varie plus en fonction du temps, le système a atteint l’équilibre.
La différence de niveaux de liquide entre les deux réservoirs génère une pression hydrostatique qui équivaut exactement à la pression osmotique. De fait, la pression osmotique est définie comme la pression hydrostatique nécessaire pour arrêter le flux de solvant au travers d’une membrane semi-perméable qui sépare deux solution de concentrations différentes.
Si, lorsque le solvant s’écoule de la solution la plus diluée vers la solution plus concentrée, avec l’objectif d’égaler les deux concentrations , on exerce une légère pression dans la solution la plus concentrée, le flux diminue au travers de la membrane.
Si l’on augmente progressivement la pression exercée, on parvient à un point où le flux au travers de la membrane est zéro, c’est-à-dire que le solvant cesse de traverser la membrane. La pression qui s’exerce à ce moment est égale à la pression osmotique. Et si la pression exercée est augmentée, le flux s’inverse et le solvant traverse la membrane dans la direction contraire, c’est-à-dire qu’il passe du côté de la solution la plus concentrée vers le côté où se trouve la solution la plus diluée. Ce processus reçoit le nom d’osmose inversée.
Donc, l’osmose inversée consiste à séparer le dissolvant d’une solution concentrée, lequel passe au travers d’une membrane semi-perméable, grâce à l’application d’une pression, laquelle devra être supérieure, au minimum, à la pression osmotique. Plus la pression appliquée est forte, plus le flux de perméat au travers de la membrane sera important.
Ce processus est particulièrement attrayant grâce à la sélectivité élevée des membranes, lesquelles permettent le passage du solvant, mais seul les ions et les molécules de petite taille dissouts dans la solution peuvent passer.
Sélectivité de la membrane
L’osmose inversée est une technique très efficace et compétitive pour séparer un solvant des solutés qui sont dissous, car, appliquée à l’eau, la membrane permet la séparation de 95 % des sels dissous, ce qui permet le dessalement des eaux salubres ou des eaux de mer.
Les membranes semi-perméables, qui laissent passer sélectivement le solvant et empêchent le passage des solutés, jouent un rôle essentiel dans le processus. Les premières étaient fabriquées en acétate de cellulose, mais ensuite, le polyamide l’a remplacé, ce qui a permis de contrôler la taille du pore et la perméabilité.
Les membranes sont peu perméables aux ions et aux molécule avec des charges électrostatiques ; plus la charge est élevée, plus la rétention est importante. Au contraire, les gaz dissous (oxygène, dioxyde carbone, chlore, etc.) ont une bonne perméabilité, comme les molécules organiques neutres à faible poids moléculaire.
Problèmes spécifiques d’encrassement
Le facteur principal qui menace la productivité de la membrane est son encrassement progressif.
Cela peut se produire pour diverses raisons, les plus communes étant:
-
Les dépôts, à la surface de la membrane, d’écailles ou de croûtes de carbonate de calcium, de sulfate de calcium, de silicates complexes, de sulfate de baryum, de sulfate de strontium, de fluorure de calcium, etc., en fonction de la composition de l’alimentation et en conséquence du fait que les concentrations en sel dans le concentré peuvent dépasser le produit de solubilité du sel.
-
Les sédiments de particules comme les colloïdes, les produits de la corrosion du fer des conduits, les précipités d’hydroxyde de fer, les algues, etc.
-
Le bio-encrassement dû à la croissance de microorganismes à la surface de la membrane, puisque certains matériaux de la membrane, comme l’acétate de cellulose ou les polyamides, peuvent être un substrat utilisable pour les microorganismes.
-
L’encrassement dû à des composés organiques comme des huiles ou des graisses présentes dans les eaux usées industrielles.
La technique de nettoyage des membranes dépend des caractéristiques de l’eau d’alimentation, du type de membrane et de la nature de l’encrassement. En règle générale, il est possible d’alterner des périodes de rinçage des membranes, en faisant circuler les solutions de nettoyage à grande vitesse en surface des membranes, avec des périodes où les membranes sont immergées dans les solutions de nettoyage.
Les agents nettoyants généralement utilisés sont:
- Acides chlorhydriques, acides phosphoriques ou citriques et agents de chélation comme l’EDTA, pour éliminer les croûtes de précipités salins, et acide oxalique pour éliminer les sédiments de fer.
- Alcalis combinés à des tensioactifs pour éliminer des microorganismes, des sédiments et des composés organiques
- Stérilisation des membranes avec des solutions de chlore pour éliminer les microorganismes.
Les nettoyages successifs finissent par dégrader les membranes. En fonction de l’application, la période de vie garantie par le fabricant est d’environ 1 – 2 ans. Avec le bon programme de nettoyage, la vie des membranes peut être prolongée jusqu’à 3 ans, une durée de vie de 5 ans étant improbable.
Généralement, pour allonger la vie des membranes l’eau d’alimentation est généralement prétraitée. Il est habituel que, en tant qu’étapes préalables à l’osmose inversée, d’effectuer d’abord un filtrage et ensuite un ultrafiltrage, toujours en fonction de la quantité de solides en suspension contenue dans les eaux à traiter.

Applications générales
L’objectif des stations de RO installées est distribué de la manière suivante:
- 50 % en dessalement d’eau de mer et d’eau salubre
- 40 % dans la production d’eau ultrapure pour les industries électronique, pharmaceutique et de production d’énergie
- 10 % en tant que systèmes de décontamination des eaux urbaines et industrielles.
Dessalement des eaux salubres
La salinité de ce type d’eaux est de 2000 mg/L – 10000 mg/L. Pour son traitement on utilise des pressions de 14 bar – 21 bar afin d’obtenir des coefficients de rejet supérieurs à 90 % et à obtenir des eaux avec des concentrations salines inférieures à 500 mg/L, qui sont les valeurs recommandées par WHO comme condition de potabilité.
Les stations de traitement des eaux salubres utilisent des modules de membranes enroulées en spirale. On estime que les coûts de capital de ce type de stations sont de l’ordre de 0.25 $US/L d’eau traitée par jour, les coûts d’exploitation étant du même ordre.
Dessalement d’eau de mer
En fonction de la zone géographique, la salinité de ce type d’eaux est de 30000 mg/L – 40000 mg/L. Pour obtenir des conditions de potabilité, on utilise des membranes en polyamide de type fibre creuse qui permettent d’obtenir des coefficients de rejet supérieurs à 99.3 % avec des pressions de travail de 50 bar – 70 bar.
Les coûts d’exploitation de ce type de stations de traitement sont estimés à 1 – 1.25$US/ L d’eau traitée/jour, ce qui rend ce système de traitement non compétitif, comparé à d’autres systèmes comme les processus d’évaporation multi étape, si les besoins en eau dépassent les 40 000 m3 d’eau traitée/jour.
Production d’eau ultrapure
La RO permet d’obtenir à partir de l’eau de consommation (concentration de solides dissous < 200 mg/L) eau de la qualité exigée dans l’industrie électronique.
Le principal problème de ce type d’installations est le bio-encrassement des membranes, il est donc nécessaire d’installer des systèmes de stérilisation par radiation UV.
Traitement des eaux usées
Cette application de la RO est limitée par les coûts élevés d’exploitation à cause des problèmes d’encrassement des membranes.
Dans le cas des eaux usées industrielles, la RO est utilisée dans les industries où il est possible d’améliorer l’économie du processus grâce à la récupération de composants de valeur qui puissent être recyclé dans le processus de production: industries de galvanoplastie et de peinture de structures métalliques, ou lorsque la réutilisation de l’eau traitée signifie une réduction importante de la consommation de l’eau, comme dans l’industrie textile.
Dans le cas des eaux urbaines, la RO est un traitement qui serait indiqué en tant que traitement tertiaire, car il est possible d’obtenir de l’eau avec une qualité qui la rendrait apte à la consommation, avec un coût de 0.5 – 0.75 $US/m3.
Le principal problème pour la consolidation de ce type de traitement est la réponse sociale. Cependant, dans certaines régions du Japon et de la Californie, il existe des limitations d’eau extrêmes, on utilise des station de RO pour traiter l’eau en provenance du traitement biologique es eaux domestiques, en utilisant l’eau traitée par RO pour la recharge des aquifères.
Applications industrielles
Les applications industrielles de cette technologie sont autant diverses qu’indispensables. Parmi les utilisations et les applications les plus répandues, on trouve les suivantes:
Industrie alimentaire, pharmaceutique et similaires
Dans les industries alimentaire, pharmaceutique, médicale, cosmétique, chimique, électronique, biotechnologique, etc. on utilise de l’eau d’osmose car pour une grande variété de processus, il est nécessaire de disposer d’une eau de grande qualité ou ultrapure. L’eau d’osmose est le point de départ pour l’obtention d’eau ultrapure.
Industrie productrice d’eau pour consommation humaine
À de nombreux points de la planète, il n’existe pas suffisamment d’eau douce ou avec la qualité nécessaire pour pouvoir approvisionner la population.
Que ce soit un problème de qualité (eaux salubres, eaux contaminées avec nitrates, métaux, pesticides, etc.) ou de quantité (en cas de recours au dessalement de l’eau de mer) l’option la plus économique pour obtenir de l’eau apte à la consommation humaine est l’osmose inversée.
Réutilisation des eaux usées
Il existe de nombreux cas dans lesquels les effluents des processus de traitement des eaux usées doivent être traitées afin d’améliorer leur qualité jusqu’à ce qu’elles puissent être réutilisées.
C’est le cas des processus qui consomment un grand débit d’eau, comme dans l’industrie textile, ou lorsque l’effluent est versé en milieu naturel pour recharger un aquifère.
C’est aussi le cas des processus qui cherchent à ne pas produire de déversement liquide (déversement zéro) et la totalité des effluents sont traités et récupérés pour être réutilisés.
Toutes les zones mentionnées pour l’utilisation de l’osmose inversée et ses applications sont couvertes par Condorchem Envitech.