Was ist Kristallisation?
Kristallisation ist ein Trennverfahren, bei dem ein Feststoff (Kristall oder Niederschlag) aus einer homogenen Phase, entweder flüssig oder gasförmig, gebildet wird. Der erhaltene Feststoff kann sehr rein sein, weshalb die Kristallisation auf industrieller Ebene als Reinigungsverfahren eingesetzt wird. Andererseits ist die Kristallisation von salzhaltigem Wasser oder die Solebehandlung eine sehr häufige Anwendung in industriellen Prozessen, die Abwasser erzeugen.

Damit die Kristallisation stattfinden kann, ist es unerlässlich, dass die Lösung übersättigt ist. Kristallisationsprozesse unterscheiden sich in der Methode, mit der die Übersättigung erreicht wird. Im Allgemeinen gibt es drei Hauptarten:
- Übersättigung durch Abkühlung der Lösung mit vernachlässigbarer Verdampfung.
- Übersättigung durch Lösungsmittelverdampfung mit geringer Abkühlung.
- Verdampfung durch Kombination von Abkühlung und Verdampfung in adiabatischen Verdampfern (Vakuumkristallisatoren).
Es ist zu beachten, dass zur Verwendung von Kristallisatoren, bei denen die Übersättigung durch Abkühlung erreicht wird, die gelösten Stoffe eine Löslichkeitskurve aufweisen müssen, die mit der Temperatur deutlich abnimmt. In Fällen, in denen die Löslichkeit kaum von der Temperatur abhängt, wird die Übersättigung durch Verdampfung des Lösungsmittels erreicht. Und bei der Kombination von Abkühlung und Verdampfung wird eine Lösung unter Vakuumbedingungen gesetzt, sodass das Lösungsmittel plötzlich verdampft und die Lösung adiabatisch abkühlt.
Diese letzte Methode ist die in der Industrie am häufigsten verwendete, um Übersättigung zu induzieren. In der Praxis gibt es eine große Vielfalt an industriellen Kristallisatoren, die jeweils speziell dafür ausgelegt sind, die Übersättigung der Lösung je nach deren Eigenschaften und Merkmalen optimal zu erreichen.
Wie funktioniert der Kristallisationsprozess?
Der Kristallisationsprozess ist nicht einfach, und die wichtigste Phase besteht darin, feste Kristalle innerhalb der flüssigen Lösung zu bilden. Die Lösung wird konzentriert und abgekühlt, bis die Konzentration des gelösten Stoffes höher ist als die Löslichkeit bei dieser Temperatur, und der gelöste Stoff bildet nahezu reine Kristalle.
Die Wachstumsrate eines Kristalls wird als Kristallisationsrate bezeichnet. Das Wachstum beginnt mit der Bildung des Keims und setzt sich dann allmählich fort. Wenn die Konzentration die Übersättigung überschreitet, erfolgt die Keimbildung – die Bildung von Keimen – natürlich, spontan und schnell. Die Kristallisationsrate kann durch die folgende empirische Gleichung ausgedrückt werden:
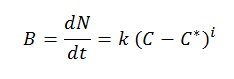
Wo:
- B: Keimbildungsrate (gebildete Keime pro Zeiteinheit und Lösungsmittelvolumen)
- N: Anzahl der gebildeten Keime pro Lösungsmittelvolumen
- t: Zeit
- k, i: empirische Parameter
- (C-C*): Übersättigung
- C: Konzentration des gelösten Stoffes in der Lösung
- C*: Sättigungskonzentration des gelösten Stoffes
Aus der Gleichung folgt, dass die Keimbildungsrate direkt von der Übersättigung abhängt. Es wurde gezeigt, dass bei hoher Übersättigung sowohl die Keimbildungsrate als auch die Kristallwachstumsrate hoch sind, was zu kleinen, unvollkommenen Kristallen mit Verunreinigungen führt. Umgekehrt ist bei niedriger Übersättigung die Bildungsrate gering, das Kristallwachstum regelmäßig und die resultierenden Kristalle sind groß und sehr rein.

Die Kristallisation umfasst hauptsächlich zwei Schritte: Keimbildung und Kristallwachstum. Beide Prozesse finden, wenn die Bedingungen günstig sind, im übersättigten Bereich des Diagramms statt. Die Keimbildung erfordert jedoch eine höhere Übersättigung als das Wachstum. Der Bereich der Keimbildung, in dem Übersättigung auftritt, wird als instabile Zone bezeichnet, während der Wachstumsbereich als metastabile Zone bekannt ist. Für die Keimbildung muss die Lösung die instabile Zone erreichen. Dort wachsen die Keime jedoch zu schnell, und die resultierenden Kristalle sind zahlreich und sehr klein. Um möglichst große und reine Kristalle zu erhalten, muss die Anzahl der sich bildenden Keime kontrolliert werden. Wenn die Lösung keine Verunreinigungen oder Kristalle derselben Art enthält, kann der Keim nur durch homogene Keimbildung entstehen. Sind Fremdpartikel vorhanden, wird die Keimbildung erleichtert, und der Prozess wird als heterogene Keimbildung bezeichnet. Sowohl homogene als auch heterogene Keimbildung treten in Abwesenheit von Kristallen derselben Lösung auf und werden zusammen als primäre Keimbildung bezeichnet. Sekundäre Keimbildung bezieht sich auf den Kristallbildungsprozess, der durch das Vorhandensein von Partikeln derselben Phase im übersättigten System bedingt und verursacht wird.
Anwendungen der Kristallisation
Der Kristallisationsprozess hat zahlreiche industrielle Anwendungen, und das Ziel, reine Kristalle zu erhalten, ist nicht immer gegeben. Kristallisatoren werden oft als Teil einer umfassenderen Behandlung von flüssigen Abwässern eingesetzt. In diesem Fall besteht das Hauptziel darin, die im Abwasser vorhandenen Verunreinigungen vom Lösungsmittel selbst zu trennen, sodass das reine Lösungsmittel gewonnen wird und die Verunreinigung in eine feste Form überführt wird, was die Handhabung wirtschaftlicher macht. Diese Kristallisationsanwendung ist beispielsweise in Null-Flüssigstoff-Ablassprozessen (Zero Liquid Discharge) von wesentlicher Bedeutung, bei denen das Abwasser in zwei Ströme getrennt wird: einen relativ reinen Lösungsmittelstrom, der für die Wiederverwendung geeignet ist, und einen anderen mit Verunreinigungen in fester oder halbfester Form.
Somit zeichnet sich die Kristallisation auch als ausgezeichnete Lösung in Fällen aus, in denen das Hauptziel nicht darin besteht, ein Feststoffprodukt hoher Reinheit zu erhalten, wie in den folgenden Anwendungen:
- Behandlung von Abwässern mit hoher Schadstoffbelastung
- Behandlung von Abwässern, wenn konventionelle Techniken nicht wirksam sind (wie bei Sole)
- Unfähigkeit, behandelte Abwässer einzuleiten
- Behandlung von Abwässern mit stark variabler Zusammensetzung
Heutzutage sind Kristallisatoren zur Behandlung von Abfallsole sehr kosteneffizient. Der Energieverbrauch wurde optimiert und reduziert, während sie eine sehr langlebige und zuverlässige Technologie im Betrieb bleiben.
