Abschnitte
Einführung
Die chemischen Elemente, die als Seltene Erden oder Lanthanoide bekannt sind, befinden sich in der Periode, die Lanthan entspricht. Sie werden üblicherweise als Seltene-Erden-Oxide unter der Bezeichnung ETR oder REE, Rare Earth Elements, ausgedrückt. Diese Elementgruppe besteht aus 15 Elementen mit sehr ähnlichen chemischen Eigenschaften, die sich jedoch in ihren physikalischen Eigenschaften unterscheiden, was ihre Trennung erschwert.
Diese Elementreihe zeigt aufgrund ihrer elektronischen Konfiguration die Lanthanoidkontraktion. Dies bedeutet die allmähliche Abnahme der Atomgröße mit zunehmender Ordnungszahl. Die Ordnungszahl dieser Elemente variiert von Nummer 57 (La) bis 71 (Lu), und diese Gruppe umfasst auch Sc (21) und Y (39) (Puche, Cascales, Porcher und Maestro) (Gambogi und Curier, 2010).
Die elektronische Konfiguration dieser Elemente zeigt, dass ihr stabilster Oxidationszustand trivalent ist, obwohl auch +2 (Eu, Yb, Sm) und +4 (Ce, Pr, Tb) Zustände stabilisiert werden können. Aufgrund ihrer elektronischen Verteilung weisen sie besondere magnetische und optische Eigenschaften auf, die beispielsweise beim Neodym (leistungsstarke Magnete) hervorgehoben werden.
Seltene Erden umfassen 17 chemische Elemente, darunter die 15 Lanthanoide (Lanthan, Cer, Praseodym, Neodym, Promethium, Samarium, Europium, Gadolinium, Terbium, Dysprosium, Holmium, Erbium, Thulium, Ytterbium und Lutetium) sowie Scandium und Yttrium, die aufgrund ihrer physikochemischen Ähnlichkeiten mit den Lanthanoiden (hauptsächlich ihre elektronische Konfiguration, Ionisationspotenziale, stark elektropositiver Charakter und Ähnlichkeit im Ionenradius (+3)) einbezogen werden, wodurch Seltene Erden in vielen Mineralien untereinander sehr austauschbar sind (durch eine Metallverdrängungsreaktion).
Seltene Erden werden in drei Gruppen eingeteilt: leichte Seltene Erden (LREEs), schwere Seltene Erden (HREEs) und die mittlere Seltene-Erden-Gruppe (MREEs), die von Samarium bis Gadolinium reicht.
Quellminerale
Es gibt etwa 200 Minerale in der Natur, die Seltene Erden in ihrer Zusammensetzung enthalten. Typischerweise treten Assoziationen verschiedener Elemente im selben Mineral aufgrund ihrer ähnlichen chemischen Eigenschaften auf. Cer ist das Seltene-Erden-Element mit dem höchsten Anteil in der Erdkruste (mehr als Kupfer), während Neodym und Lanthan häufiger vorkommen als Nickel, Blei und Kobalt.
Derzeit sind die wichtigsten Erze der Seltenen Erden Monazit [(Ce, La, Th) PO4], Xenotim [(YPO4)3] und Loparit (Na,Ce,Sr)(Ce,Th)(Ti,Nb)2O6 als Erz geringerer Qualität (Puche, Cascales, Porcher und Maestro).
Monazit ist ein Phosphatmineral mit der Formel [(,,,ℎ)4], das das zweitwichtigste Erz der LREEs darstellt und Reserven in Australien, Brasilien, China, Indien, Sri Lanka und den Vereinigten Staaten aufweist. Lagerstätten mit Monazit enthalten oft Thorium, ein radioaktives Element, weshalb viele Länder es als Quelle für Seltene Erden aufgrund potenzieller Umweltschäden ablehnen.
Die Konzentrationen der Seltenen Erden und von Thorium im Monazitmineral variieren je nach Lagerstätte, mit einem Durchschnitt von 70 % Seltene Erden (hauptsächlich Cer, Neodym und Lanthan) und 12 % Thorium (auch Urananteile können vorkommen, das wie Thorium ein radioaktives Element ist).
Monazit ist ein Orthophosphat der Seltenen Erden und Thorium (RTh)PO4. Es ist das häufigste Mineral der Seltenen Erden und ein Nebenprodukt von Ilmenit, das mit Zirkon einhergeht.
Bastnäsit ist ein Fluorkarbonat (RFCO3), das Seltene Erden enthält, insbesondere Ce, Nd, Eu und La. Die wichtigsten Reserven befinden sich in der Mongolei und Kalifornien.
Dieses Fluorkarbonatmineral mit der Formel [(,)3(,)] kommt in Lagerstätten in China und den Vereinigten Staaten vor und entspricht den größten Reserven an leichten Seltenen Erden (hauptsächlich Lanthan, Cer und Neodym) weltweit. Sie enthalten sehr geringe Thoriumkonzentrationen, und ihr Gehalt an Seltenen Erden beträgt etwa 70 %.
Xenotim ist ein Orthophosphat der Seltenen Erden und Yttriums mit hohem Gehalt an Cer und Thorium. Die wichtigste Lagerstätte dieses Minerals befindet sich in Guangdong (China), obwohl sein Uran- und Thoriumgehalt sowie die damit verbundene Radioaktivität die Ausbeutung einschränken. Weitere weniger bedeutende Lagerstätten befinden sich in Kalifornien (USA), Malaysia und Indonesien.
Euxenit ist ein Mineral mit der Formel [(,,,,ℎ)(,,)26]. Es wird üblicherweise als Tantalniobat (Minerale, in denen Ta und Nb die Verbindung bilden) von Titan, Seltenen Erden, Thorium und Uran gefunden. Lagerstätten existieren in Idaho (USA), Norwegen und Madagaskar.
Loparit ist ein Niob-Titanat der Seltenen Erden auf der Kola-Halbinsel, Russland, mit Konzentraten von etwa 32 % Seltene-Erden-Oxiden, hauptsächlich Cer.
Xenotim ist das wichtigste Mineral der HREEs weltweit, speziell von Yttrium. Es enthält durchschnittlich 67 % Seltene Erden, und die wichtigsten Lagerstätten weisen einen Xenotim-Gehalt von 0,5–5 % auf. Lagerstätten dieses Minerals befinden sich in Kalifornien (USA), Malaysia und Indonesien.
Allanit ist ein Mineral mit der chemischen Formel [(,,)(22+)(//4) ∙ 27]. Es gehört zur Epidot-Gruppe (ein Silikatmineral mit der allgemeinen Formel 23(4)3(,), wobei A und B durch verschiedene Elemente ersetzt werden können) und liegt in drei Formen vor, die Cer, Lanthan und Yttrium enthalten.
Es kommt in magmatischen, metamorphen und hydrothermalen Umgebungen vor. Der Anteil radioaktiver Elemente (Thorium und Uran) kann von Spuren bis zu 3 % variieren, während die Konzentration der Seltenen Erden durchschnittlich etwa 5 % beträgt.
Aufgrund des Vorhandenseins von radioaktiven Elementen und seiner geringen Konzentration an Seltenen Erden wird es nicht als primäres Mineral im Bergbau gewonnen.
Abschließend ist eine bestimmte Art von Tonen, die reich an Seltenen Erden sind, als wichtiger Speicher hervorzuheben. Diese speziellen Tone entstehen durch Verwitterung gewöhnlicher magmatischer Gesteine, die Seltene Erden enthalten, was zur Auslaugung dieser Gesteine und anschließenden Absorption an der Oberfläche von tonigen Aluminiumsilikatmineralien (Kaolinit, Illit und Smektit) führt, wodurch sie mit Seltenen Erden angereichert und wirtschaftlich abbaubar werden.
Obwohl die Konzentrationen der Seltenen Erden in der Regel niedrig sind (durchschnittlich 0,3 %) im Vergleich zu den oben beschriebenen Mineralien, ist die Verarbeitung dieser Lagerstätten weniger komplex, was sie wirtschaftlich wettbewerbsfähig macht.
Diese Lagerstätten existieren in Südchina und Kasachstan. Obwohl Tonreserven nur 2,9 % der Reserven in China ausmachen, repräsentieren sie 35 % der Seltenen-Erden-Exporte des Landes.
Speziell in China (Xungu, Longnam) gibt es Reserven von mehr als 10 Mio. Tonnen ausgedrückt als RO (Seltene-Erden-Oxide). Diese oberflächennahen Lagerstätten in China sind relativ leicht abzubauen und sehr profitabel.
Seltene-Erden-Ionen werden durch Ionenaustausch in den Kristallgittern der Tone adsorbiert. Seltene Erden werden aus der Auslaugung der Tone mit Salzlösungen zurückgewonnen. 50 % der weltweiten Reserven an Seltenen Erden befinden sich in China.
Die derzeit industriell eingesetzten Verfahren zur Rückgewinnung zielen darauf ab, ETR-Konzentrate aus den genannten Mineralien zu gewinnen. Mit Ausnahme von Bastnäsit werden viele ETR-Konzentrate als Nebenprodukte oder Ergebnisse pyrometallurgischer oder hydrometallurgischer Prozesse gewonnen (Orrego, 1998; Orrego, 2000; Vega, 2000; Hedrick, 1999; Dwivedi, 1982; Harrah, 1967; Sunur et al., 1985; Alarcon, 1998; Lapido, 1994; Sundaram, 1987; Swanina und Nair, 1989; The Humphreys Investment Co, 1970).
Technologische Eigenschaften
Weltweit sind Seltene Erden Elemente, die dank ihrer physikalischen und chemischen Eigenschaften in einer Reihe von Hightech-Produkten Verwendung finden. Zunächst gewinnt die Permanentmagnetindustrie in Medizintechnologien (Kernspintomographie, PET), Elektroniktechnologien, Mobilitätstechnologien (Eisenbahn), Hybridtechnologien usw. zunehmend an Bedeutung.
Ursprünglich wurden Permanentmagnete aus Stählen hergestellt, ferritische Metalllegierungen mit niedriger Remanenz und Koerzitivfeldstärke. Seltene Erden bieten hohe Koerzitivfeldwerte und magnetische Momente, die die von ferritischen Magneten übertreffen.
Der Schwachpunkt der Seltenen Erden liegt bei Raumtemperatur im Paramagnetismus. Dieser Punkt wurde jedoch durch die Legierungen Sm2Co17 und insbesondere die neueren Nd2Fe34B mit magnetischer Energie von 450 KJ/m3 überwunden. Ebenso wurden GdTbFeCo-Legierungen als sehr effizient in Speichersystemen entdeckt.
Die technologische Nutzung der Seltenen Erden im Bau optischer Materialien ist ein weiteres aktuelles Einflussfeld. Konkret handelt es sich um den Bau von Dreifarb-Lampen, bei denen das ausgestrahlte Licht eine Kombination aus drei Wellenlängen ist: 450 nm; Ba Mg2O16 Al27 Eu2+/556 nm; (Ce/Tb)Mg Al11 O19/610 nm; Y2O3Eu3+. Diese lumineszenten Systeme reproduzieren Sonnenlicht und erreichen eine sehr hohe Lichtausbeute.
In diesem Zusammenhang ist die Verwendung von Seltenen Erden in der Technologie von RX-Verstärkerfolien klassisch. Traditionell wird Calciumtungstat (CaWO4) verwendet.
Diese lumineszenten Materialien zielen darauf ab, die Strahlenexpositionszeit des Patienten zu reduzieren und eine korrekte Auflösung zu erreichen. Diese Materialien werden durch andere ersetzt, um die Effizienz zu verbessern. Gd2O2ScTb+, LaOBrTm+ und YTaO.
Ebenso reproduzieren Fernsehbildschirme, Computermonitore und Mobilbildschirme Farben aus mit Lanthaniden dotierten Chromophorgruppen. Die rote Farbe wird beispielsweise durch mit Europium dotiertes Yttriumoxysulfid (Y2O3:Eu3+) erzeugt. Ein weiteres Anwendungsfeld der Seltenen Erden sind Laser, insbesondere hocheffiziente Neodym-Laser mit Monochromatizität, Kohärenz und Richtwirkung. (Sáez, Cascales, Porcher, Maestro; 2000).
Extraktionsprozess
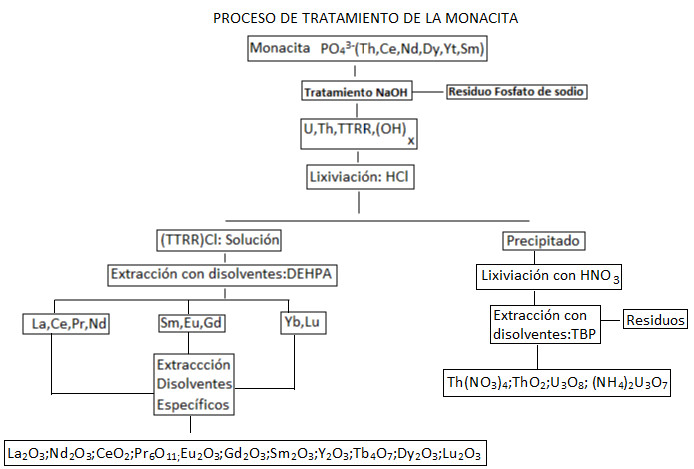
Monazit
Eines der wichtigsten Seltene-Erden-haltigen Minerale wird als Referenz herangezogen: Monazit.
Ausgehend vom Monazitkonzentrat wird dieses mit Schwefelsäure bei einer Temperatur von 200 ºC behandelt, um die Lanthanoide, die Teil des Konzentrats sind, auszulaugen.
Im Prozess werden auch Verunreinigungen wie Uran, Thorium, bestimmte Phosphate und Sulfate gelöst, was die Gewinnung eines sekundären Konzentrats dieses radioaktiven Materials ermöglicht. Die Lösung wird langsam neutralisiert.
Zunächst erfolgt eine Behandlung mit Ammoniumhydroxid. Bei pH-Werten von 1 fällt Thoriumsulfat in seiner unlöslichen Form aus. Zusammen mit Thoriumsulfat fällt ein kleiner Teil der Seltenen Erden aus. Bei einem pH-Wert von 2,3 fällt der Großteil der Seltenen Erden aus.
Schließlich fällt bei einem pH von 6 Uran als Hydroxyuranat aus. Die bei pH 1 und 6 anfallenden Niederschläge werden mit Tributylphosphat behandelt, um Uran von den Seltenen Erden zu trennen und den Ertrag des Prozesses zu verbessern. An diesem Punkt wird ein Seltene-Erden-Konzentrate gewonnen.
Durch Zugabe von Natriumsulfat erfolgt die Fällung der leichten Seltenen Erden (REE), was ergibt;
2(4)3 ∙ 24 ∙ 2
Yttrium, schwere Seltene Erden und radioaktive Elemente verbleiben in Lösung. Der Niederschlag wird nach der Abtrennung mit Natriumhydroxid behandelt, um ein Seltene-Erden-Konzentrate zu bilden. Dieses wird bei 120 ºC getrocknet.
Der Niederschlag wird in Salpetersäure wieder aufgelöst, und Thorium sowie Cer werden durch Zugabe von Ammoniumhydroxid bei pH 2,8 selektiv gefällt.
Anschließend wird nach Entfernung dieses ersten Niederschlags kontinuierlich Ammoniumhydroxid zugegeben, wodurch der Rest der Seltenen Erden als Hydroxide ausfällt. Die schweren Seltenen Erden in Lösung können von anderen radioaktiven Elementen getrennt und mit einem Extraktionsmittel wie Tributylphosphat konzentriert werden.
Zur Rückgewinnung von Thorium und Seltenen Erden aus der Lösung wird die saure Lösung mit Natriumoxalat behandelt, wodurch Thorium und Seltene Erden bei pH 1,5 ausfallen, während Uran in Lösung verbleibt. Der Oxalatniederschlag wird mit Natriumhydroxid behandelt, wodurch die Seltenen Erden ausfallen.
Dieser Niederschlag wird kalziniert und mit Salpetersäure behandelt, um die Seltene-Erden-Extraktion wieder aufzulösen und zu reinigen. Diese saure Lösung wird mit Tributylphosphat behandelt, wodurch ein organischer Extrakt mit Thorium und Cer und eine Lösung mit Seltenen Erden entsteht.
Der Extrakt wird einer Reinigungsstufe mit Natriumnitrit unterzogen, wobei Ceriumnitrat in der wässrigen Phase und Thoriumnitrat in der organischen Phase erhalten wird.
Tone
Das größte Volumen an gewonnenen Seltenen Erden stammt aus Tonlagerstätten in China. Der Gehalt an Seltenen Erden ist nicht hoch, aber die einfache Gewinnung begünstigt den Abbau. Diese Einfachheit beruht auf der ionischen Form, mit der Lanthanoidionen mit der Silikatstruktur des Tons interagieren.
Seltene Erden liegen in kationischer Form (+3) vor und sind leicht extrahierbar. Der Extraktionsprozess basiert auf der Verwendung konzentrierter Lösungen von einwertigen Kationen (Na2SO44)2SO44Cl).
Bei der Wechselwirkung findet ein Ionenaustausch zwischen den einwertigen Ionen und den Lanthanoidionen statt. Die Seltenen Erden gehen als Sulfate und/oder Chloride in Lösung.
Diese Lösung wird mit Natriumoxalat behandelt, sodass unlösliche Oxalate der Lanthanoide gebildet werden, die in der Lösung ausfallen. Dieser Oxalatniederschlag wird bei 900 ºC kalziniert, um die Oxide zu erhalten. Dieses Oxidkonzentrat gewinnt zwischen 80 und 90 % der in der ursprünglichen Tonerde enthaltenen Seltenen Erden zurück.
In Madagaskar wird Meerwasser verwendet, um die Tone auszulaugen und anschließend die Seltenen Erden mit Oxalaten auszufällen.
Trenn- und Reinigungsprozesse
Die technologische Nutzung dieser Materialien erfordert einen hohen Reinheitsgrad bei der Gewinnung. Dies hat zur Entwicklung neuer, effektiverer Extraktionssysteme als die traditionellen geführt.
Seltene Erden können mit Nitraten, Chloriden und Sulfaten ausgelaugt werden. Sobald ein Seltene-Erden-Konzentrate gewonnen wurde, muss ein Trenn- und Reinigungsprozess eingeleitet werden.
Selektive Oxidation
Zunächst kann eine selektive Oxidation durchgeführt werden, indem Cer, Praseodym und Terbium vom (+3)-Zustand in den (+4)-Zustand oxidiert werden. Im Fall von Praseodym kann bei Oxidation unter hohem Sauerstoffdruck die Zusammensetzung PrO2 erreicht werden.
Praseodym und Terbium sind in wässriger Lösung im tetravalenten Zustand nicht stabil, was es relativ einfach macht, sie aus einer Lösung von Seltene-Erden-Hydroxiden (gebildet durch Auflösen der Oxidmischung mit Kaliumhydroxidlösung) mit Kaliumchlorat (KClO3) als Oxidationsmittel auszufällen.
Cer ist das häufigste Seltene-Erden-Element und daher das mit dem geringsten kommerziellen Wert. Es kann durch Erhitzen der Oxidmischung auf 650 ºC an der Luft oder durch Trocknen von Seltene-Erden-Hydroxiden an der Luft bei 120–130 ºC in den tetravalenten Zustand oxidiert werden.
In wässrigen Lösungen, in denen die Elemente als Hydroxide gelöst sind, kann Cer durch Chlorierung oder Elektrolyse oxidiert werden. Cer kann auch in Lösung durch Injektion von Ozon als Oxidationsmittel oxidiert werden. Um oxidiertes Cer (tetravalenter Zustand) zurückzugewinnen, kann die Mischung der Seltenen Erden selektiv in verdünnter Säure gelöst werden, in der Cer(IV)-Oxid eine geringe Löslichkeit aufweist.
Das schwarze Oxid löst sich in Säure unter Sauerstofffreisetzung und bildet grüne Lösungen oder grüne Salze, die in der Keramikindustrie Anwendung finden.
Elemente wie Samarium, Europium und Ytterbium sind weniger häufig als Cäsium; daher müssen sie vor der chemischen Behandlung zur Rückgewinnung konzentriert werden. Europium (III) kann mit einer Quecksilberkathode zu Europium (II) reduziert werden. Die Rückgewinnung von Samarium kann aus Lithiumamalgamen erfolgen.
Superkritisches Extraktionsverfahren
Lanthan, Neodym, Samarium, Europium, Gadolinium, Dysprosium und Holmium-Karbonate können aus einem Seltene-Erden-Extrakt gewonnen werden, indem eine wässrige Suspension der Oxide mit CO2 bei einer Temperatur von mindestens 31 ºC und einem Druck von 71,2 atm behandelt wird.
Unter diesen Bedingungen bilden sich die Karbonate Pr (III), Er(III), Yb(III) und Tb(III) nicht oder nur mit sehr geringem Ertrag. Diese Trenntechnik wurde auch zur Trennung von Lanthanoiden im (III)-Oxidationszustand von denen im (IV)-Zustand verwendet.
Die Betriebsbedingungen sind 40 ºC und 100 atm, wobei nach einer Stunde Reaktionszeit die Karbonate von Lanthan, Neodym, Samarium, Europium, Holmium, Promethium und Thulium im (III)-Oxidationszustand gebildet werden. So entsteht ein karbonatischer Niederschlag, der abgetrennt und mit Salzsäure behandelt werden kann. Diese Lösung kann mit Lösungsmitteln oder Ionenaustauschharzen behandelt werden.
Lösungsmittel-Extraktion
Ausgehend von einem Seltene-Erden-Konzentrate, das aus der Auslaugungsstufe gewonnen wurde, wird die Lösungsmittel-Extraktionsstufe gespeist. In dieser Stufe werden schwere Seltene Erden (Terbium, Dysprosium, Holmium, Erbium, Thulium, Ytterbium, Lutetium und Yttrium), mittlere (Samarium, Europium und Gadolinium) und leichte (Lanthan, Cer, Praseodym und Neodym) getrennt.
Anschließend wird durch Extraktion mit spezifischen Lösungsmitteln jedes spezifische Seltene-Erden-Oxid getrennt. Schließlich erfolgen Reinigungen mittels Ionenaustausch- oder chromatographischer Techniken. Die wichtigsten Extraktionsmittel im Bereich der Seltenen Erden sind;
- Carbonsäuren. Dies sind erschwingliche Säuren mit moderaten Preisen, trotz des Nachteils ihrer Wasserlöslichkeit. Zu den am häufigsten verwendeten Carbonsäuren gehören Versatinsäure 10, Naphthensäuren und 2-Bromdecanonsäure, alle in Xylol verdünnt. Die Löslichkeit der Naphthensäure variiert je nach pH-Wert. Bei pH 4 beträgt die Löslichkeit 0,09 g/l und variiert bis zu 0,9 g/l bei pH 6,5. Die Löslichkeit der Versatinsäure reicht von 0,7 g/l bis 0,25 g/l. Die 2-Bromdecanonsäure wirkt bei sauren Werten. Der sterische Effekt des Säuremoleküls beeinflusst die Extraktion der Lanthanoide und steht im Zusammenhang mit der Ordnungszahl des Metallelements.
- Alkylphosphorsäuren. Die am häufigsten verwendete Säure ist DEHPA (Di-2-ethylhexylphosphorsäure). Diese Säure wird in Kerosin verdünnt verwendet. Zum Beispiel HCl 0,1 M mit einer Lösung von DEHPA 0,2 M in Kerosin. Es wird beobachtet, dass die Extraktion dieser Elemente in der Reihenfolge La < Ce < Nd < Sm < Eu < Gd < Tb < Dy = Y < Ho < Er < Tm < Yb < Lu verbessert wird, wobei der Verteilungskoeffizient mit steigender Temperatur abnimmt. Eine weitere Alkylphosphorsäure, die verwendet wird, ist EHEHPA (2-Ethylhexyl-2-ethylhexylphosphorsäure), ebenfalls in Kerosin verdünnt. Eine verwendete Formulierung ist HCl 0,1 M und die Konzentration des Extraktionsmittels in Kerosin 0,2 M. In diesem System nimmt die Metall-Extraktion mit der Ordnungszahl zu, ist jedoch geringer als im DEHPA-System. Die Verwendung von Phosphonsäuren und/oder Phosphinsäuren verbessert die Trennung zwischen benachbarten Lanthanoiden.
- Hydroxylamine. Speziell saure Agenzien mit Chelatbildner-Fähigkeit. Diese Extraktionsmittel wurden häufig bei der Behandlung von Cu verwendet, aber ihre Anwendung bei der Behandlung von Seltenen Erden nimmt zu. Zum Beispiel wurde SME 529 (heute LIX 84) verwendet, um das Extraktionsgleichgewicht von Ce(III) und La(III) in einem Natriumchloridmedium zu untersuchen, wobei das Extraktionsmittel in n-Heptan verdünnt war. LIX 70 wurde ebenfalls für die Extraktion dieser beiden Seltenen Erden verwendet. In diesem Fall wurden Kerosin und n-Heptan als Verdünnungsmittel für die organische Phase getestet, wobei das wässrige Medium NaCl war. Sowohl Cer als auch Lanthan werden quantitativ extrahiert, obwohl Cer bei niedrigeren pH-Werten extrahiert werden kann.
Die Art der Amine und das wässrige Medium beeinflussen die Extraktion dieser Elemente entscheidend. Primäre Amine (RNH2) extrahieren diese Metalle aus einem Sulfatmedium, während tertiäre Amine (R3N) sie aus einem Nitratmedium extrahieren.
Im Allgemeinen werden leichte Seltene Erden bevorzugt mit diesen basischen Extraktionsmitteln extrahiert.
- TBP (Tributylphosphat) und DBBP (Di-n-butyl-n-butyl-phosphonat). Seltene Erden werden aus verschiedenen wässrigen Medien extrahiert. Mit ihnen werden Europium und Samarium gewonnen. Ihr Wirkungsmechanismus basiert auf der Reaktion: Ln3+aq + 3NO3– + 3Lorg < => Ln(NO3)3L3(org)
- Crown-Ether. Sie wurden zur Extraktion von Lanthanoiden verwendet. (sim-dibenzo-16-crown-5-oxyessigsäure) in einer 80:20 Chloroform-Heptanol-Lösung. Bei Crown-Ethern hängt die Extraktion verschiedener Seltenen Erden sehr spezifisch vom pH-Wert des wässrigen Mediums ab, sodass Lu3+ bei pH 6,7 quantitativ extrahiert wird, während La3+, Pr3+, Sm3+, Eu3+, Tb3+, Er3+ und Yb3+ bei pH 6,5 nahezu quantitativ (> 98 %) extrahiert werden. Die Stöchiometrie des extrahierten Komplexes ist 1:2 (Metall: Extraktionsmittel). Calixarene sind (1,n)-Cyclophane, die eine von Phenylgruppen gebildete Kavität besitzen, die als Brücken wirken und die Einführung von Substituenten in das organische Gerüst ermöglichen. Diese Struktur hat dazu geführt, dass diese Verbindungen als Reagenzien zur Extraktion einiger trivalenter Lanthanoide untersucht werden.
- Lanthan, Neodym, Europium, Erbium und Ytterbium.
- Synergistische Mischungen. Synergistische Mischungen ersetzen traditionelle Extraktionssysteme mit einem einzelnen Extraktionsmittel. Synergistische Mischungen, die Kombinationen von zwei oder mehr Extraktionsmitteln sind, die die Effektivität der Extraktion erhöhen und die Spezifität der Trennoperation verbessern, gewinnen zunehmend an Bedeutung. Zum Beispiel wurde eine Phosphonsäure wie PC-88 A (2-Ethylhexylphosphonsäure) in n-Heptan zusammen mit DTPA (Diethylamin-pentaessigsäure) für die Extraktion von Lanthanoiden untersucht.
Die Trennfaktoren zwischen Y/Ho/Er sind größer, wenn DTPA hinzugefügt wird, während die Stöchiometrie der extrahierten Spezies durch LnR3-3HR dargestellt wird.
Schlussfolgerungen
Seltene Erden waren vor einigen Jahren einfach das Ende des Periodensystems, das aus Zeitmangel oder schlicht Unwissenheit nicht erreicht wurde. Heutzutage haben ihre technologischen Eigenschaften und industriellen Anwendungen diese Minerale für viele Regierungen zu kritischen Mineralien gemacht.
In der Executive Order 13817 vom 20. Dezember 2017 erkennt die US-Regierung die Verwundbarkeit an, die die externe Abhängigkeit von 35 als kritische Mineralien eingestuften Mineralien für ein technologisches System darstellt, von denen 17 Seltene Erden sind.
Sie zeichnen sich durch hohe elektrische Leitfähigkeit und magnetische Eigenschaften aus, die sie optimal für die Herstellung von Batterien, Mobiltelefonen, Batterien für Elektrofahrzeuge, LED-Beleuchtungssystemen, Windturbinen, Lasersystemen, Satellitentechnologien, Verteidigungssystemen usw. machen.
Diese Anwendungen erfordern Reinheit der gewonnenen Metalle und effektive Behandlung der Konzentrate. Neue Methoden wie die Anwendung von Crown-Ethern, die Verwendung synergistischer Mischungen wie Kombinationen von Alkylphosphorsäuren oder die Anwendung von quartären Ammoniumsalzen werden die Optimierung des Anreicherungsprozesses erleichtern.
Literaturverzeichnis
F.J. Alguacil und F. Rodríguez, CSIC. Verfahren zur Trennung von Seltenen Erden. Rev. Metal Madrid, 33 (3), 1997
Bautista, R.G. Mineral Proc. Extractive Met. Rev., 8, 1992: 175-182.
Bautista, R.G. und Jackson, N. Seltene Erden, Ressourcen, Wissenschaft, Technologie und Anwendungen. TMS. Warrendale (USA), 1992.
Habashi, F. Rare Earths’90. Proc. Int. Symp. on Processing of Rare Metals. Osaka (Japan), 1990: 47-52.
Patricio Javier Avendaño Corvalán, Dissertation „EVALUATION OF TECHNICAL-ENVIRONMENTAL FEASIBILITY OF A RARE EARTH EXTRACTION PLANT IN CHILE“ Fakultät Chile, 2017
R. Sáez Puche, C. Cascales, P. Porcher, P. Maestro. „Rare Earths: Advanced Materials“. Fakultät für Chemische Wissenschaften, Complutense Universität Madrid. CSIC. CNRS. Chemische Forschung. 2000
