Què és la cristal·lització?
La cristal·lització és un mètode de separació en què es produeix la formació d’un sòlid (cristall o precipitat) a partir d’una fase homogènia, líquida o gasosa. El sòlid format pot arribar a ser molt pur, per la qual cosa la cristal·lització s’empra a nivell industrial com a procés de purificació. D’altra banda, la cristal·lització d’aigües que contenen sals, o tractament de salmorres, és una aplicació molt habitual en processos industrials que generen aigües residuals.

Perquè la cristal·lització es pugui dur a terme és condició indispensable que la solució es trobi sobresaturada. Els processos de cristal·lització difereixen uns d’uns altres en el mètode mitjançant el qual s’aconsegueix la sobresaturació. En general, es pot aconseguir de tres maneres diferents:
- Sobresaturació produïda per refredament de la solució amb evaporació despreciable.
- Sobresaturació produïda per evaporació del dissolvent amb poc refredament.
- Evaporació per combinació de refredament i evaporació en evaporadors adiabàtics (cristal·litzadors al buit).
Cal tenir present que per utilitzar els cristal·litzadors en què la sobresaturació s’aconsegueix mitjançant refredament, els soluts han de tenir una corba de solubilitat que disminueixi significativament amb la temperatura. En aquells casos en què la solubilitat no depèn pràcticament de la temperatura, la sobresaturació s’aconsegueix evaporant el dissolvent. I quan s’utilitza la combinació de refredament i evaporació, una solució es sotmet a condicions de buit perquè el dissolvent s’evapori de manera sobtada i la solució s’enfredi adiabàticament.
Aquest últim mètode és el més utilitzat a nivell industrial per provocar la sobresaturació. A la pràctica, existeix una àmplia varietat de cristal·litzadors industrials, cadascun dissenyat específicament per aconseguir de forma òptima la sobresaturació de la solució, en funció de les característiques i propietats d’aquesta.
Com funciona el procés de cristal·lització?
El procés de cristal·lització no és senzill i l’etapa més important consisteix en la formació de cristalls sòlids en el si de la solució líquida. La solució es concentra i s’enfreda fins que la concentració del solut és superior a la solubilitat a dita temperatura i el solut forma cristalls gairebé purs.
La velocitat de creixement d’un cristall es coneix com a velocitat de cristal·lització. El creixement ocorre primer amb la formació del nucli i després el seu creixement es va produint de forma gradual. Quan la concentració és superior a la sobresaturació, la nucleació –formació de nuclis– es produeix de forma natural, espontània i ràpida. La velocitat de cristal·lització es pot expressar mitjançant la següent equació empírica:
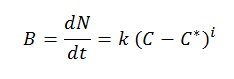
On:
- B: velocitat de nucleació (nuclis formats per unitat de temps i de volum de dissolvent)
- N: nombre de nuclis formats per unitat de volum de dissolvent
- t: temps
- k, i: paràmetres empírics
- (C-C*): sobresaturació
- C: concentració del solut en la solució
- C*: concentració de saturació del solut
De l’equació es dedueix que la velocitat de nucleació és funció directa de la sobresaturació. S’ha comprovat que quan la sobresaturació és elevada, la velocitat de nucleació –i també la velocitat de creixement del cristall– també són elevades, donant lloc a cristalls petits, imperfectes i amb impureses. I a l’inrevés, quan la sobresaturació és baixa, la velocitat de formació és petita, el creixement dels cristalls és regular i s’obtenen cristalls de gran mida i d’elevada puresa.

En la cristal·lització es distingeixen principalment dos passos: la nucleació i el creixement dels cristalls. Ambdós processos es produeixen, si les condicions són favorables, a la zona sobresaturada de la gràfica. No obstant això, per a la nucleació es requereix més sobresaturació que per al creixement. L’àrea de formació nuclear on es dóna la sobresaturació es denomina zona inestable, mentre que l’àrea de creixement es coneix com a zona metaestable. Per a la nucleació és necessari que la solució arribi a la zona inestable. Tanmateix, un cop allà, els nuclis creixeran massa ràpid i els cristalls resultants seran molts i molt petits. Per aconseguir la formació de cristalls tan grans i purs com sigui possible, cal controlar la quantitat de nuclis en formació. Si la solució no conté impureses ni cristalls del seu propi tipus, el nucli només pot ser format per nucleació homogènia. Si algunes partícules estranyes estan presents, la nucleació es facilita i el procés és conegut com a nucleació heterogènia. Ambdues nucleacions, la homogènia i la heterogènia, tenen lloc en absència de cristalls de la pròpia solució i són col·lectivament conegudes com a nucleació primària. La nucleació secundària es refereix al procés de formació de cristalls que està condicionat i produït per la presència de partícules de la mateixa fase en el sistema sobresaturat.
Aplicacions de la cristal·lització
El procés de cristal·lització té nombroses aplicacions industrials i no sempre es persegueix obtenir cristalls purs. Els cristal·litzadors són utilitzats sovint com a part d’un tractament més ampli d’efluents líquids. En aquest cas, l’objectiu principal és la separació de la contaminació present en un efluente del propi dissolvent, de manera que s’obtingui el dissolvent pur i la contaminació en forma sòlida, per facilitar-ne la gestió de forma econòmica. Per exemple, aquesta aplicació de la cristal·lització és indispensable en els processos de vessament zero, en què l’efluent es separa en dos corrents, la del dissolvent relativament pur i apte per a la seva reutilització, i la de la contaminació en estat sòlid o semi-sòlid.
Així doncs, la cristal·lització també es presenta com una excel·lent solució en aquells casos en què l’objectiu principal no és l’obtenció d’un producte sòlid d’elevada puresa, com passa en les següents aplicacions:
- Tractament d’efluents amb una elevada càrrega contaminant
- Tractament d’efluents quan les tècniques convencionals no són efectives (com en el cas de les salmorres)
- Impossibilitat de poder vessar els efluents tractats
- Tractament d’efluents la composició dels quals fluctua i és molt variable
Actualment, es pot disposar de cristal·litzadors per al tractament d’aigües amb sals que són molt competitius pel que fa a eficiència energètica, ja que es basen en una evaporació al buit per bomba de calor, i molt robustos pel que fa al seu funcionament.
